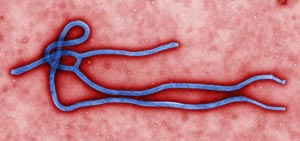
El virus de Ébola no se transmite por el aire. No infecta a través del aire.El virus se transmite principalmente a través del contacto directo con fluidos corporales. Una persona infectada solo puede infectar a otras cuando los síntomas son evidentes (como la fiebre), y es muy poco probable que el virus de Ébola evolucione de forma que pueda contagiarse a través del aire.

Por Jesús Sáinz Maza
Científico
Sin embargo, se sabe muy poco de los mecanismos de infección. No sabemos qué fluidos corporales son los que contienen el virus, ni sabemos si los objetos que toca una persona infectada son contagiosos.
Los datos son escasos debido a que todas las epidemias que ha habido antes de la actual terminaron antes que el número de personas infectadas llegara a 500. Los estudios de los que disponemos sugieren que las principales vías de transmisión incluyen el contacto con una persona infectada, compartir una cama, y el contacto con fluidos corporales. En los funerales africanos de enfermos de Ébola hay un riesgo extremadamente alto de contagio debido a los rituales que implican tocar el cuerpo, lavarse las manos conjuntamente, y las comidas comunales.
Un estudio sugiere que el sudor puede desempeñar un papel importante en la transmisión. Pero el análisis más completo realizado hasta la fecha indica que los factores de riesgo difieren dependiendo de la etapa de la enfermedad, y que las personas infectadas que están en las etapas tardías de la enfermedad son mucho más propensas a transmitir el virus. La infección es poco probable que pueda darse por un apretón de manos con una persona infectada o al tocar el pomo de una puerta tocado por un infectado. Sin embargo, no se sabe si los métodos utilizados en los estudios realizados tienen la capacidad de detectar virus en concentraciones muy bajas.
En conclusión, parece ser que sabemos demasiado poco de los mecanismos de infección de una enfermedad tan letal como para haber traído a España a una persona infectada. ¿Dimitirá alguien de algún cargo político?
RECUPERANDO MATERIALES
Por Jesús Sáinz Maza
Del genoma al fármaco
(Publicado en 2006)
El primer paso consiste encontrar una marca genética asociada a la enfermedad. Para ello se utilizan marcadores conocidos y marcadores nuevos diseñados mediante análisis bioinformático del genoma. Aunque hay millones de marcadores conocidos no siempre son suficientes. El mayor riesgo de diabetes lo detectamos con el marcador DG10S478 de nuevo diseño. Los marcadores, lugares variables del genoma, se utilizan fundamentalmente en dos tipos de estrategias, la de ligamiento en la que se analizan familias, y la de asociación en la que se analizan individuos sin relación familiar. En ambos casos se trata de encontrar variantes genéticas que sean significativamente más frecuentes en los enfermos que en los individuos sanos. El paso siguiente es la replicación de los resultados en otras poblaciones. Los resultados obtenidos en una población no son necesariamente válidos en otra. Cada población tiene patrones genéticos diferentes, y tanto los marcadores asociados a enfermedades como los genes que las causan pueden variar. Al marcador de riesgo de diabetes, DG10S478, lo validamos en las poblaciones islandesa, danesa y estadounidense. No sabremos si detecta riesgo en la población española hasta que se haya hecho el análisis experimental.
Para el desarrollo de fármacos es necesario definir el gen que está implicado en la enfermedad. La estructura genómica en la región del marcador define los genes candidatos. La cercanía del gen al marcador es uno de los criterios más importantes. El gen responsable se define mediante análisis de la función biológica de los candidatos. La caracterización funcional se obtiene mediante una multitud de técnicas de laboratorio que definen la expresión del gen, las proteínas que codifica, los procesos moleculares en los que está implicado, etc. Los resultados nos permiten saber qué gen está implicado en la enfermedad. Por ejemplo, al gen ALOX5AP lo pudimos relacionar con aumento de la producción de leucotrienos, unas moléculas que a su vez encontramos aumentadas en los afectados de infarto de miocardio.
Una vez definido el gen responsable de la enfermedad, empieza el proceso de generación del fármaco. Para ello se analiza la proteína o proteínas que codifica. No todas las proteínas son susceptibles de ser controladas mediante fármacos. Se estima que menos del 5% son buenas dianas farmacológicas. Los fármacos son mayoritariamente compuestos químicos que tiene que ser solubles, fáciles de administrar y, por supuesto, no tóxicos. Cuando se empiezan los ensayos clínicos en seres humanos, la información obtenida mediante los análisis genéticos tiene un gran valor. Permite seleccionar los pacientes con la marca genética de riesgo. Eso da mayores garantías de que en estos pacientes la enfermedad tiene el origen molecular para el cual se ha diseñado el fármaco.