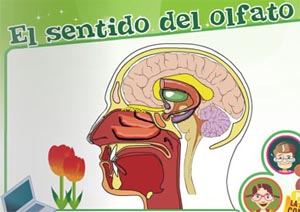
Se ha propuesto recientemente la posibilidad de usar el sentido del olfato como herramienta para diagnosticar la enfermedad de Alzheimer, Parkinson y otras enfermedades degenerativas del sistema nervioso.
Se ha observado en numerosos pacientes de dichas enfermedades una pérdida del sentido olfatorio mucho antes que aparezcan los síntomas típicos de la enfermedad. Las pruebas para detectar la capacidad olfativa son sencillas de usar y de conseguir.
La ventaja de usar estas pruebas, no solo reside en la anticipación para detectar la enfermedad sino también en la posibilidad de eliminar diagnósticos erróneos. Hay casos en los que se ha diagnosticado erróneamente alguna de estas enfermedades degenerativas del cerebro y se ha observado que no había pérdida olfativa. Es decir, la validación de la prueba olfativa serviría para disminuir el número de diagnósticos incorrectos.
Es interesante observar que muchos factores de riesgo a padecer enfermedades neurodegenerativas son también factores de riesgo para la pérdida del olfato. Por ejemplo, la edad es un factor de riesgo para la enfermedad de Alzheimer o Parkinson, y es común en las personas de edad avanzada la pérdida de olfato. Golpes en la cabeza y la exposición crónica a ambientes polucionados y metales ionizados son factores de riesgo para ambas enfermedades y para la pérdida de capacidad olfativa.
Hay numerosos estudios, durante la última décadas, que han encontrado una asociación entre la pérdida de la capacidad olfativa con la degeneración cerebral. Cierto es que la capacidad predictiva no es muy elevada, sin embargo supera la de otros marcadores biológicos hoy utilizados para tratar de predecir el desarrollo de la degeneración del sistema nervioso. Otro problema es la falta de especificidad de la prueba olfativa, la cual es capaz de predecir el desarrollo de la degeneración cerebral pero no es capaz de definir el tipo de enfermedad degenerativa.
La complejidad de las enfermedades neurodegenerativas, en las cuales hay evidencias e indicios que apuntan a una multitud de factores como responsables de su desarrollo, hacen difícil el diagnóstico. Para comprender por qué se asocia la pérdida de olfato a la degeneración del sistema nervioso es necesario clarificar antes muchos interrogantes. No se sabe siquiera si los defectos molecular conocidos de las enfermedades neurodegenerativas son la causa de la pérdida del olfato, o si dicha pérdida ocurre antes de dichos daños moleculares y está relacionada con la degeneración mediante otros mecanismos moleculares. Esperemos que una gestión y financiación adecuada permita desarrollar dicha investigación científica.

RECUPERENDO MATERIALES
Por Jesús Saínz Maza
Del genoma al fármaco
(Publicado en Enero de 2006)
El primer paso consiste encontrar una marca genética asociada a la enfermedad. Para ello se utilizan marcadores conocidos y marcadores nuevos diseñados mediante análisis bioinformático del genoma. Aunque hay millones de marcadores conocidos no siempre son suficientes. El mayor riesgo de diabetes lo detectamos con el marcador DG10S478 de nuevo diseño. Los marcadores, lugares variables del genoma, se utilizan fundamentalmente en dos tipos de estrategias, la de ligamiento en la que se analizan familias, y la de asociación en la que se analizan individuos sin relación familiar. En ambos casos se trata de encontrar variantes genéticas que sean significativamente más frecuentes en los enfermos que en los individuos sanos. El paso siguiente es la replicación de los resultados en otras poblaciones. Los resultados obtenidos en una población no son necesariamente válidos en otra. Cada población tiene patrones genéticos diferentes, y tanto los marcadores asociados a enfermedades como los genes que las causan pueden variar. Al marcador de riesgo de diabetes, DG10S478, lo validamos en las poblaciones islandesa, danesa y estadounidense. No sabremos si detecta riesgo en la población española hasta que se haya hecho el análisis experimental.
Para el desarrollo de fármacos es necesario definir el gen que está implicado en la enfermedad. La estructura genómica en la región del marcador define los genes candidatos. La cercanía del gen al marcador es uno de los criterios más importantes. El gen responsable se define mediante análisis de la función biológica de los candidatos. La caracterización funcional se obtiene mediante una multitud de técnicas de laboratorio que definen la expresión del gen, las proteínas que codifica, los procesos moleculares en los que está implicado, etc. Los resultados nos permiten saber qué gen está implicado en la enfermedad. Por ejemplo, al gen ALOX5AP lo pudimos relacionar con aumento de la producción de leucotrienos, unas moléculas que a su vez encontramos aumentadas en los afectados de infarto de miocardio.
Una vez definido el gen responsable de la enfermedad, empieza el proceso de generación del fármaco. Para ello se analiza la proteína o proteínas que codifica. No todas las proteínas son susceptibles de ser controladas mediante fármacos. Se estima que menos del 5% son buenas dianas farmacológicas. Los fármacos son mayoritariamente compuestos químicos que tiene que ser solubles, fáciles de administrar y, por supuesto, no tóxicos. Cuando se empiezan los ensayos clínicos en seres humanos, la información obtenida mediante los análisis genéticos tiene un gran valor. Permite seleccionar los pacientes con la marca genética de riesgo. Eso da mayores garantías de que en estos pacientes la enfermedad tiene el origen molecular para el cual se ha diseñado el fármaco.